代表性成果1:开发脐血CD34+干祖细胞诱导来源iNK/CAR-iNK工程化制备技术
当前,临床使用的CAR-NK细胞主要来自工程化的外周血或脐带血等人体组织分离扩增的成熟NK细胞。然而,在成熟NK阶段进行CAR工程化引入高昂成本。本研究整合了CD34+造血干祖细胞(CD34+ HSPCs) CAR工程化、干细胞扩增和NK谱系定向诱导技术,成功建立了高效诱导脐带血造血干祖细胞体外产生iNK(induced NK)细胞及CD19 CAR-iNK细胞的工艺制备体系。经过42天的诱导,实现了将单个CD34+ HSPCs诱导输出107级别的iNK细胞或106级别的CD19 CAR-iNK细胞。相比已报道的方法,本方法可以显著提高iNK细胞或CAR-iNK细胞的诱导效率,并显著降低制备CAR-NK细胞的病毒使用量。
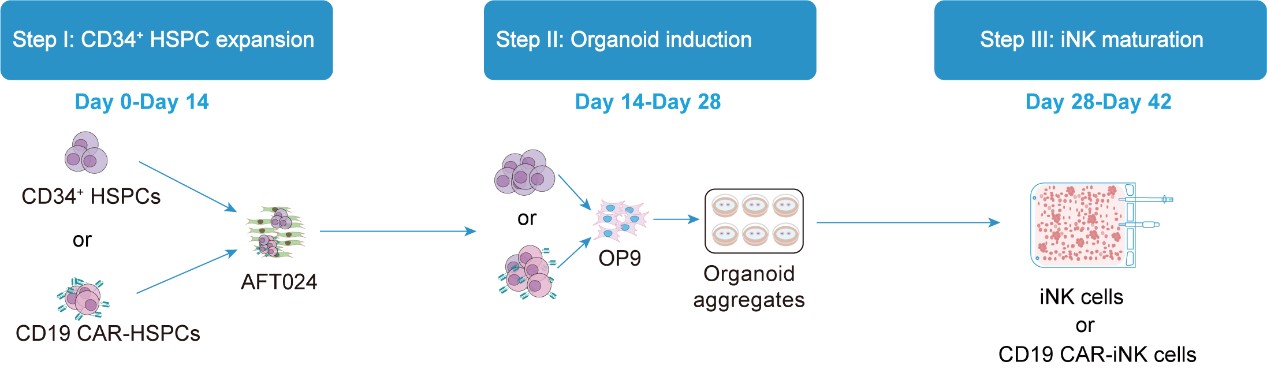
图1. 脐带血来源iNK/CAR-iNK工程化制备技术
代表性成果2:多能干细胞来源CRO-CD7 CAR-iNK细胞: 避免自相残杀,延长体内续存、有效抑制T细胞肿瘤
T细胞急性淋巴细胞白血病(T-ALL)是一种侵袭性的恶性血液肿瘤。CD7蛋白在超过95%的急性淋巴性白血病(ALL)和30%的急性髓系白血病(AML)病人中呈高表达。然而CD7蛋白也表达在正常的T细胞和NK细胞中,导致CD7 CAR-T/CAR-NK细胞间存在自相残杀。本研究通过基因编辑与基因工程成功构建敲除CD7基因并过表达CD7 CAR的CD7 KO-CD7 CAR-hESCs,类器官法诱导其分化产生了免疫表型和功能正常的CD7 KO-CD7 CAR-iNK细胞。这些细胞成功避免自相残杀,具备正常的扩增能力,对T-ALL细胞系和T-ALL病人来源细胞表现出优越的抗肿瘤活性。CD7 KO-CD7 CAR-hESCs过表达CXCR4基因后诱导产生的CRO-CD7 CAR-iNK细胞,细胞学水平上在体内外周血循环血的续存时间可延长至28天以上,并显著延长T-ALL细胞荷瘤小鼠的生存期。该研究揭示了人多能干细胞来源的CD7 KO-CD7 CAR-iNK细胞在治疗T细胞恶性肿瘤中的临床潜力,为治疗T细胞恶性肿瘤提供了一种有前景的细胞制剂。
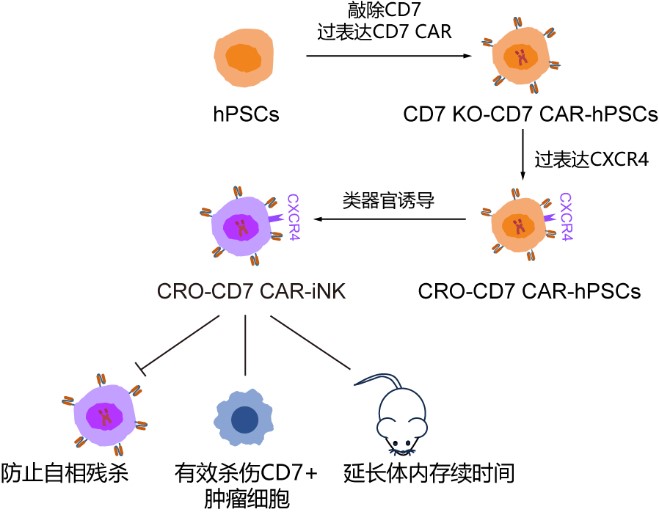
图2. 避免自相残杀、延长体内续存的CRO-CD7 CAR-iNK
(https://jhoonline.biomedcentral.com/articles/10.1186/s13045-025-01712-3)
代表性成果3:建立诱导人多能干细胞分化再生NK细胞新技术
NK细胞可以直接广谱杀伤各种肿瘤细胞,毒副作用小,过继治疗不需要配型,是理想的现货式免疫细胞治疗药物。当前临床治疗用的NK细胞主要来源于脐带血和外周血等人体组织,这些天然来源的NK细胞异质性大,制备成本高昂、产量低、制备周期受人体组织可及性限制。人类多能干细胞诱导分化来源的NK细胞有望解决上述问题。本研究首次开发出一种不依赖拟胚体形成,基于高纯度的侧板中胚层的类器官聚集体再生iNK细胞的技术方法。在27天的诱导周期内,投入百万数量级别的人类多能干细胞即可输出超过十亿数量级别的iNK细胞。该方法大幅提高了iNK细胞的成熟度,内源CD16表达比例由低于20%提高到40%~80%,诱导效率较传统EB法提高了100倍,诱导周期缩短至一个月。iNK细胞可通过直接诱导靶细胞凋亡和ADCC作用的方式杀伤人类肿瘤细胞。本研究提供了一种可规模化从人类多能干细胞诱导再生iNK细胞的技术方法,目前该研究已进入临床转化阶段。
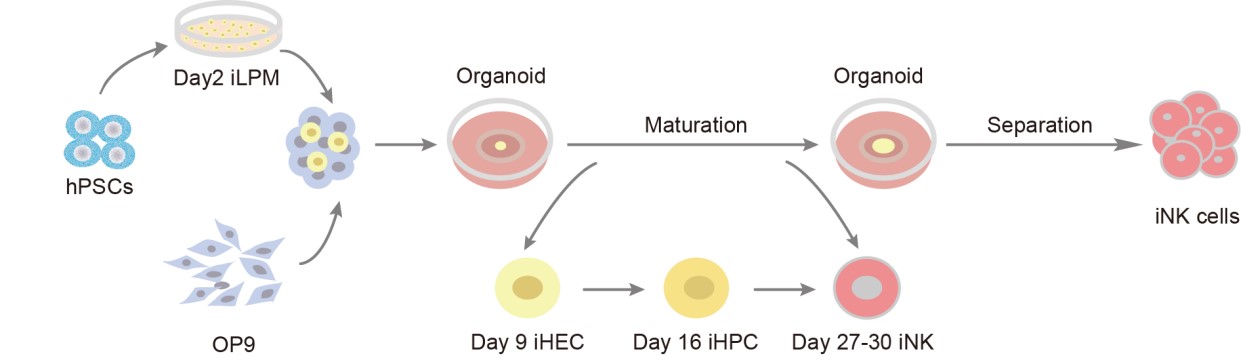
图3. 开发人类多能干细胞诱导再生NK细胞技术
(https://www.nature.com/articles/s41421-022-00467-2)
代表性成果4:建立小鼠多能干细胞分化再生多谱系血液免疫细胞技术
造血干祖细胞再生一直是实验血液学和再生医学领域的关键技术挑战。本研究筛选出关键转录因子组合并构建了Runx1、Hoxa9和Hoxa10三因子打靶的小鼠PSC,利用已建立的PSC定向分化体系,在体外分化获得造血种子细胞。这些造血种子细胞移植后能在野生型(先天和获得性免疫系统正常)受体鼠中稳定嵌合长达6个月以上时间,输出完整的髓系、B和T等谱系细胞,且未发现致瘤现象。本研究利用小鼠PSCs定向分化的方法,首次在免疫系统完备的小鼠体内实现长期稳定多谱系造血重建。本研究构建的体系稳定易重复,便于跨实验室平台测试和从事造血分化基础研究,为造血干祖细胞再生转化医学提供了重要的理论和技术支持。
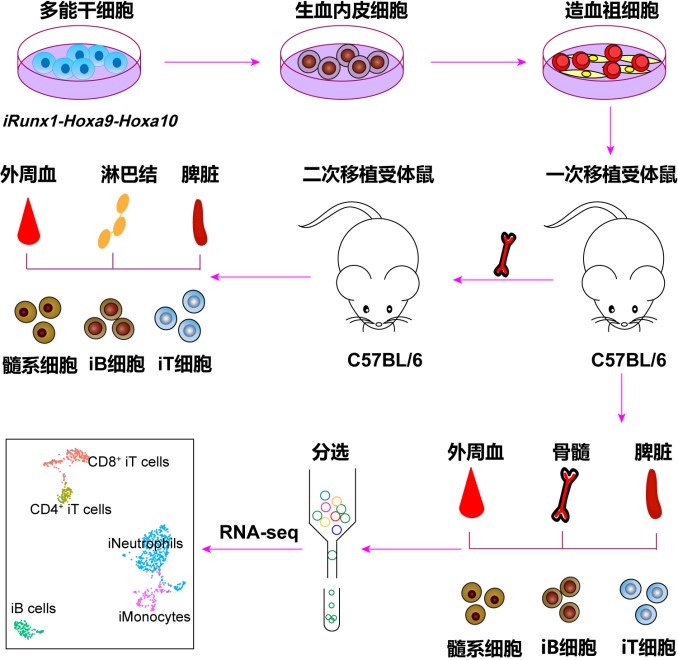
图4. Runx1、Hoxa9 和 Hoxa10 组合诱导小鼠 PSCs 分化再生多谱系血液免疫细胞
代表性成果5:多能干细胞定向分化再生B免疫谱系
B细胞是体液免疫的关键细胞成分,包括固有免疫B1细胞和获得性免疫B2细胞(MZ B, FO B)两大类群。任何一种B细胞缺陷都会导致体液免疫受损,甚至导致严重感染类疾病。对于B细胞功能低下和不全相关疾病的治疗,再生B细胞是一个理想的选择。本研究基于“体外再生种子细胞,体内发育成熟”两步法策略实现诱导B细胞再生。首先,在多潜能干细胞(PSC)中共表达Runx1、Hoxa9、Lhx2三个转录因子,通过在造血发生以及B淋系生成阶段连续作用产生造血种子,移植后利用B细胞先天缺失小鼠的体内微环境,成功在小鼠体内诱导出完整而成熟的B细胞谱系,实现抗原特异性体液免疫应答,并产生长期免疫记忆。这为开发B细胞疗法治疗B细胞相关疾病提供了理论支持和及技术借鉴。
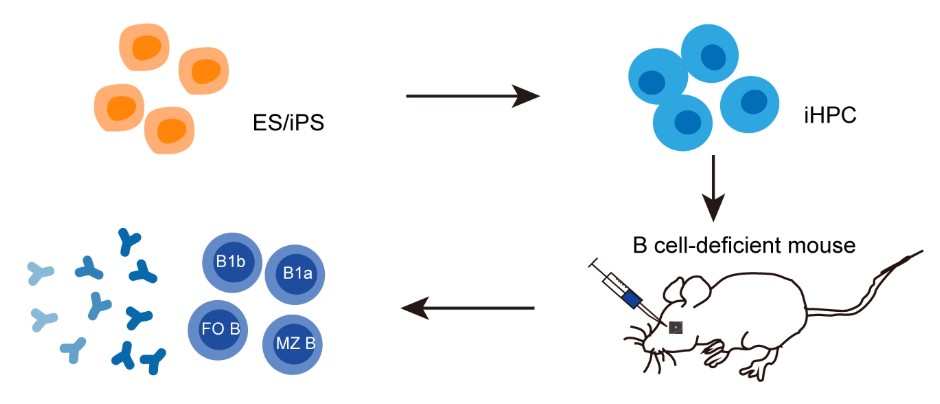
图5. 多能干细胞定向分化再生B免疫谱系
(https://www.nature.com/articles/s41423-021-00805-6)
代表性成果6:通过特定因子诱导多能干细胞再生T细胞
本研究首次报道了转录因子Runx1和Hoxa9协同表达可以高效诱导多能干细胞(PSC)定向分化产生T细胞的种子细胞,将其移植后能够在免疫缺陷鼠体内重建T免疫系统,再生途径恢复了免疫缺陷鼠的T细胞免疫监视功能。采用这种二步法再生T细胞技术方案,该研究进一步基因编辑iPSC,使之带上肿瘤相关抗原特异性TCR(TAA-TCR),成功实现体内再生肿瘤特异性TCR-T细胞,在实体瘤小鼠模型中有效遏制肿瘤生长。这种体内再生的抗肿瘤TCR-T细胞,具备Naïve表型,肿瘤抗原激活后可以产生效应T细胞和记忆T细胞。该研究利用多能干细胞为材料,重建T免疫系统,而且实现重建具有治疗意义的T细胞抗肿瘤免疫,为T细胞相关免疫缺陷(如艾滋病)和T细胞抗肿瘤等转化研究,提供了新的技术借鉴。
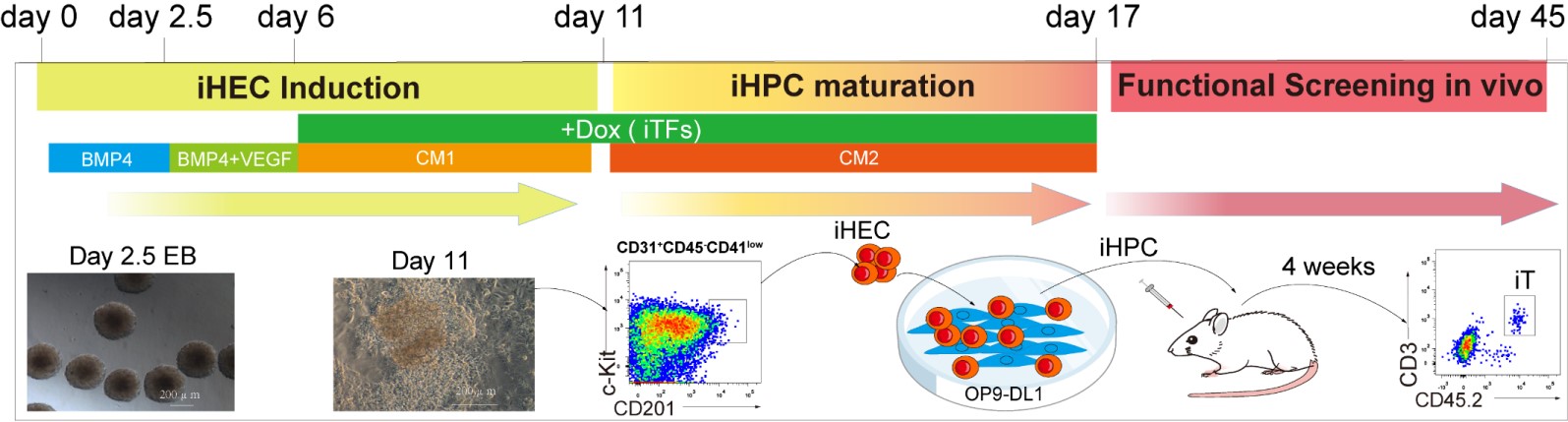
图6. 多能干细胞定向再生T细胞,实现体内抗肿瘤
(https://www.nature.com/articles/s41422-019-0251-7)
代表性成果7:在体重编程再生造血干细胞样细胞
多能造血祖细胞(Multipotent blood progenitors, MPP)由造血干细胞(Haematopoietic stem cells, HSC)分化而来,能够迅速分化产生所有成体血液谱系细胞,是维持造血稳态和应激造血的关键祖细胞。和HSC不同的是,MPP失去自我更新的能力,但增殖分化能力强大,数量也多。本研究首次揭示了Hoxb5可以体内高效诱导多能造血祖细胞重编程为具有造血干细胞样(HSC-like)的新型细胞,证明这种HSC-like的细胞可以实现在动物上三次系列移植,且具有在体内重建多谱系长期造血的能力。该研究为开发替代传统骨髓移植细胞来源提供了新的思路。
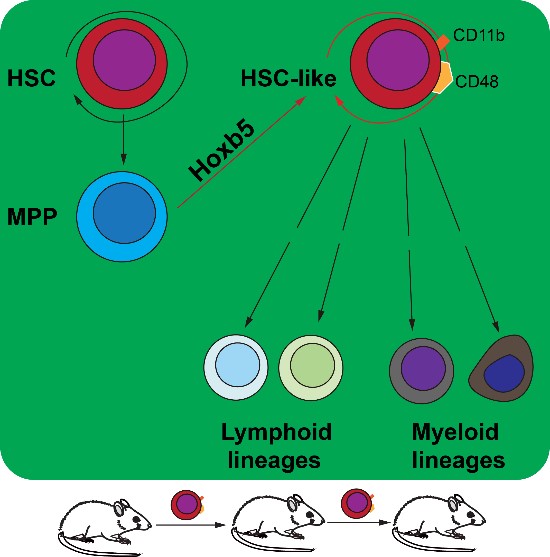
图7. Hoxb5将MPP重编程为HSC-like 细胞
(https://doi.org/10.1111/cpr.13235)
代表性成果8:Nupr1通过p53信号通路调控HSC的休眠-激活态转换
造血干细胞(HSC)具有自我更新能力并能分化为各种血液细胞。生理状态下,造血干细胞大部分处于休眠状态,仅有少量细胞增殖以维持造血稳态。这种精密的稳态维持是受到复杂的机制调控的,目前为止,HSC 休眠态与激活态的平衡调控机制尚不明确。本研究发现,转录因子 Nupr1 可以调控造血干细胞(HSC)休眠态和激活态的转换,敲除 Nupr1 的 HSC 更多的处于增殖期并具备更强的移植竞争优势。进一步转录组测序结果揭示,Nupr1-/- HSC的p53信号通路显著下调,随后将Nupr1-/- HSC中的p53表达水平回调,其竞争优势下降,说明Nupr1对HSC稳态的调节是通过p53信号通路来实现的。该研究对于寻求手段干预HSC实现扩增、干性维持、促进植入等具有重要理论指导意义。
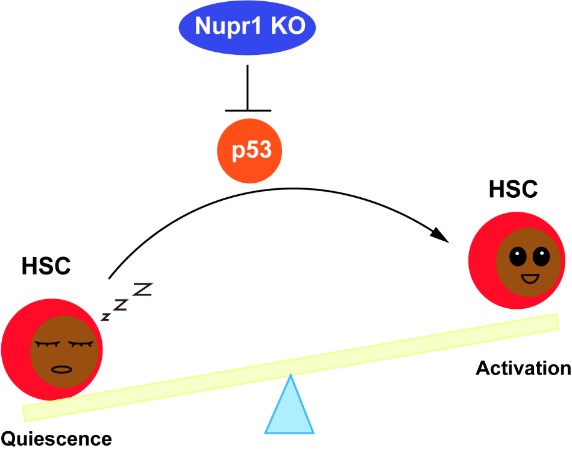
图8. Nupr1通过p53信号通路调控HSC的休眠-激活态转换
(https://haematologica.org/article/view/haematol.2019.239186)
代表性成果9:
骨髓增生异常和骨髓增殖混合型肿瘤(Myelodysplastic/Myeloproliferative neoplasms,MDS/MPN)是一种克隆性恶性血液肿瘤,常伴有骨髓间质微环境异常。目前,针对该类白血病的治疗方案主要是造血干细胞移植、化疗以及靶向药物治疗,但治疗效果欠佳。本研究建立了一种通过骨髓腔内原位输注供体间充质干细胞(MSCs)重建白血病小鼠被破坏的骨髓微环境的方法。原位输注供体MSCs可以改善白血病小鼠的造血生成,最终抑制白血病发展进程,显著延长白血病小鼠生存时间。本研究从微环境角度建立了一种骨髓间充质干细胞介导局部骨髓微环境重塑和系统性抑制白血病发展的新方法,为探索局部输注MSCs作为MDS/MPN白血病患者的候选治疗方法提供了理论依据和技术参考。
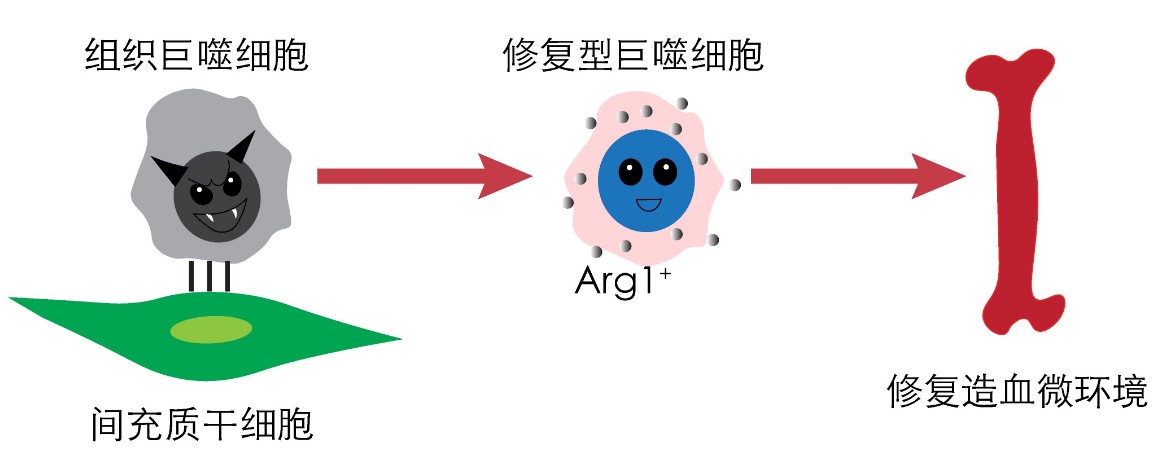
图9. 间充质干细胞赋能组织巨噬细胞修复造血微环境,遏制白血病进展
(https://www.nature.com/articles/s41375-020-0775-3)
代表性成果10:转录因子Hoxb5诱导B细胞重编程为功能性T淋巴细胞
长期以来,体外再生T细胞技术面临技术困境:体外无法成功模拟T细胞发育的胸腺微环境;体外诱导产生的T细胞种类受限,而且没有经过自体胸腺微环境的阳性、阴性筛选,产生的T细胞难以在体内发挥正常、有效的生理功能。本研究避开体外无法模拟T细胞发育胸腺微环境的技术瓶颈,建立了一种体内大规模功能筛选获得再生T细胞的技术平台。最终,成功地从15个候选转录因子中筛选鉴定到Hoxb5,可以将 pro/pre-B 细胞体内重编程为早期 T 淋巴祖细胞(early T cell progenitor, iETP),这些 iETP 细胞可以在免疫缺陷鼠体内进一步分化为各个类型的成熟的 T 细胞,执行正常的生理和免疫功能,并产生长期获得性免疫记忆。首次建立在体重编程再生功能性 T 淋巴细胞的技术,实现体内 T 淋巴免疫系统重建。该研究为基础领域研究提供了认识血液谱系命运改变的新视角, 也提供了再生T细胞临床转化新思路。
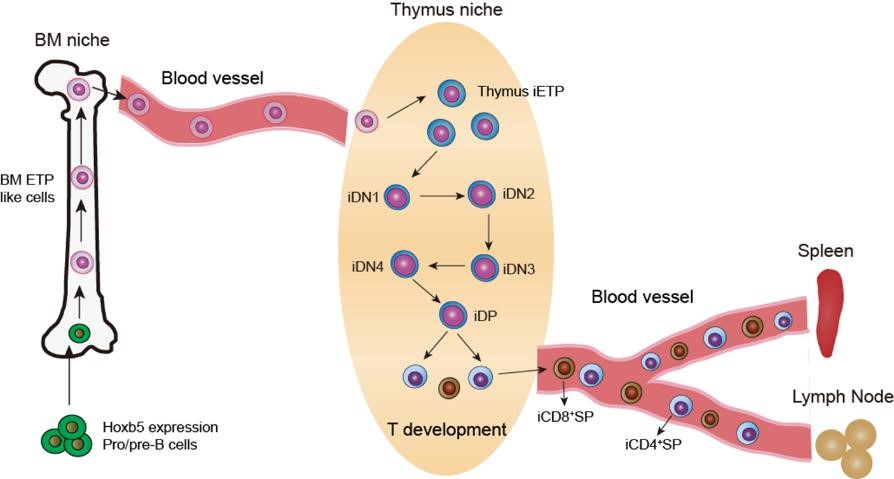
图10. 转录因子Hoxb5体内将B细胞重编程为T细胞,实现体内抗肿瘤
(https://www.nature.com/articles/s41590-018-0046-x)