1. 新型“肽基可离子化脂质”平台实现mRNA精准器官靶向递送和先导编辑
通过融合多肽(Peptide)与可离子化脂质(Ionizable Lipid)这两大类生物材料的优势,创造出一类全新的肽基可离子化脂质(Peptide Ionizable Lipid, PIL),进而建立了一种肽基脂质驱动的器官靶向mRNA递送平台——PILOT(Peptide Ionizable Lipid-driven Organ Targeting)。PILOT平台可在无需配体修饰和额外脂质加入的情况下,实现对肝、脾、肺、胸腺、骨等多器官的特异性mRNA递送。其中,肝靶向PILOT LNP递送 mRNA 的效果和安全性媲美甚至优于美国 FDA已批准剂型。此外,肝靶向PILOT LNP 和肺靶向PILOT LNP能够高效共递送先导编辑组分(PEmax mRNA和epegRNA),分别实现对肝脏和肺部的高效先导编辑。
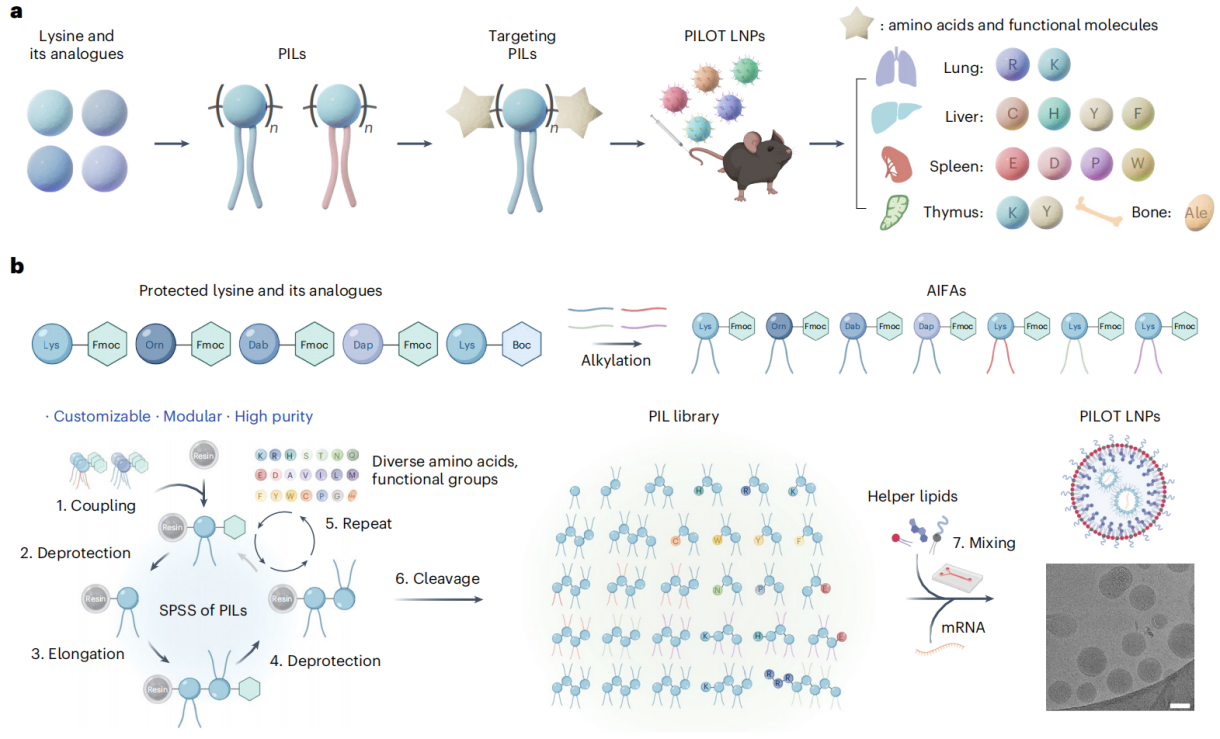
图1. PILOT平台助力实现mRNA精准器官靶向递送和先导编辑(Nat. Mater., 2025)
文章链接:https://www.nature.com/articles/s41563-025-02320-9
2. 器官和细胞双重特异性mRNA-LNP递送技术研发用于精准肿瘤治疗
通过结合基于LNP的器官靶向递送和mRNA序列的受控表达,开发了一种器官和细胞双重特异性的mRNA-LNP递送平台,简称SELECT。该平台通过系统优化开发出三组分LNPs,可以将mRNA靶向递送到肺脏、肝脏和脾脏;通过在mRNA骨架中引入特定的microRNA(miRNA)靶点的反向互补序列,实现了mRNA在靶组织特定细胞类型中的受控蛋白质表达。
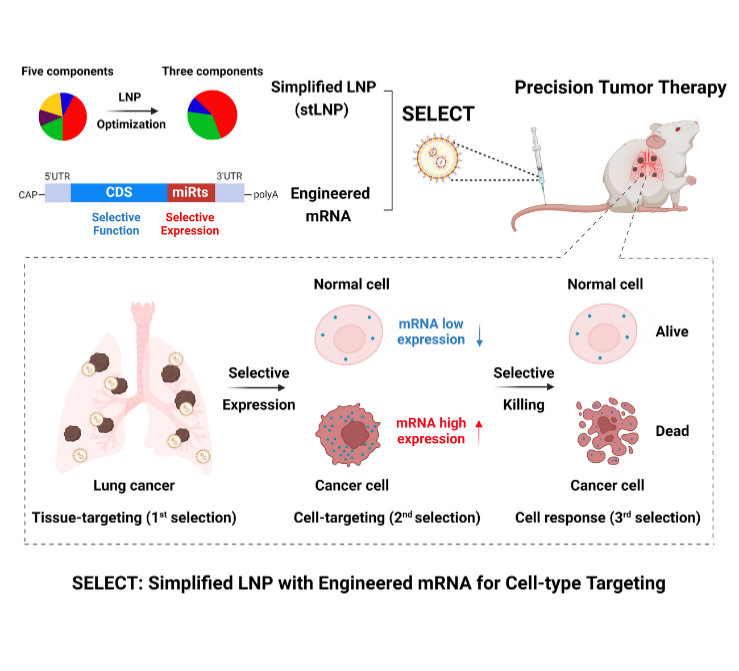
图2.器官和细胞双重特异性mRNA-LNP递送技术研发用于精准肿瘤治疗(Adv. Mater., 2024)
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202409812
3. 掺杂锰离子的脾脏靶向mRNA疫苗用于增强体内抗肿瘤免疫
针对目前mRNA疫苗抗肿瘤疗效有限的问题,开发了一种新型脾脏器官靶向的治疗性mRNA癌症疫苗.该疫苗不仅有效实现了mRNA抗肿瘤疫苗精准递送至抗原提呈细胞,还通过锰离子佐剂(Mn2+)的掺入显著提升了抗原提呈效率以及免疫激活能力,在多种肿瘤模型中均表现出良好的抑瘤效果。此外,该疫苗还具备工艺简便、安全性高等优势,为治疗性mRNA癌症疫苗的临床转化提供了有潜力的新策略。
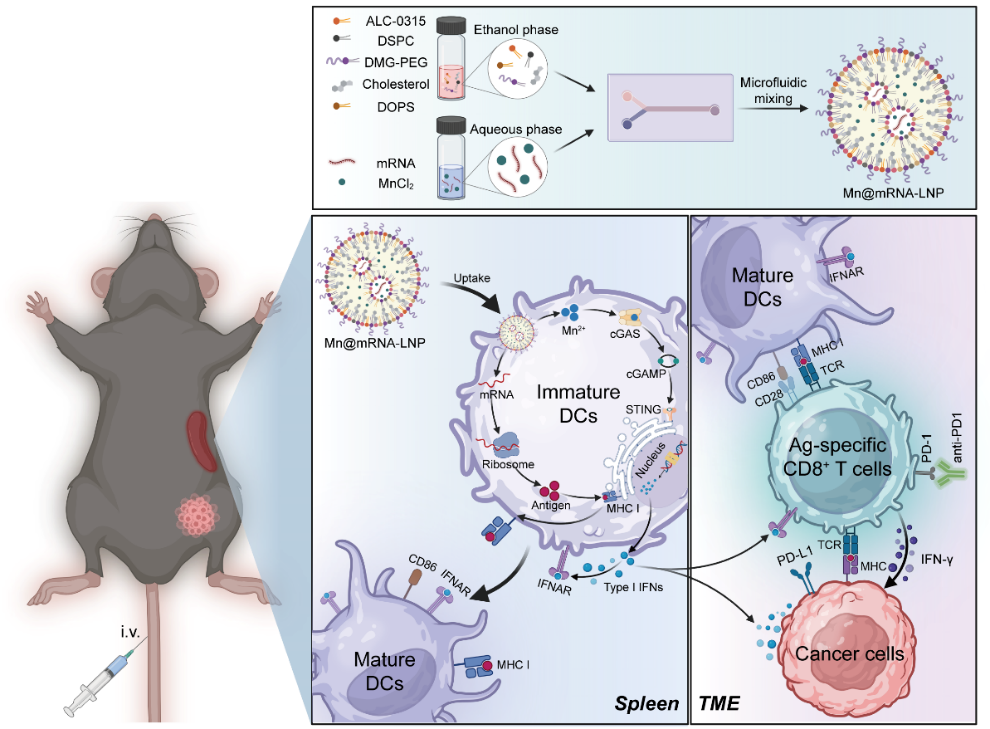
图3. 掺杂锰离子的脾脏靶向mRNA疫苗用于增强体内抗肿瘤免疫(ACS Nano, 2024)