1. 皮质下母源复合体SCMC的功能机制:我们实验室早期鉴定了一种在哺乳动物卵母细胞和早期胚胎中特异性表达的母源蛋白复合体—皮质下母源复合体SCMC,在母源向合子转变过程中发挥至关重要作用(Dev Cell 2008);持续研究表明该复合体由母源效应蛋白组成,并证明了SCMC复合体在人类中保守,同时鉴定了多个SCMC新组分(Nat Commun 2014; Mol Hum Reprod 2015; JMCB 2018; Development 2019);SCMC逐渐成为关于哺乳动物母源调控与女性生殖健康研究的前沿方向(Trends Mol Med 2017)。最近,通过冷冻电镜体外重构了SCMC核心复合体原子分辨率结构,证明了SCMC核心复合体组装异常是相关女性生殖疾病发病的主要原因,揭示了核心组分对复合体的稳定功能(Nat Struct Mol Biol 2024);还鉴定了SCMC的新组分14-3-3蛋白和SPIN1;重构了SCMC/14-3-3五元复合体结构,揭示SCMC通过其中的TLE6磷酸化调控14-3-3/CDC25B活性进而参与哺乳动物早期胚胎细胞周期(Nat Commun 2024);揭示SCMC通过维持表观调控因子SPIN1的胞质定位,确保小鼠卵母细胞向早期胚胎过程中H3K4me3重编程和ZGA的正常进行(Nat Struct Mol Biol 2025)。这些研究成果不仅为研究哺乳动物早期胚胎发育母源调控和女性生殖疾病研究开辟了新方向,还为女性生殖疾病的诊疗提供了新的标记物和策略。
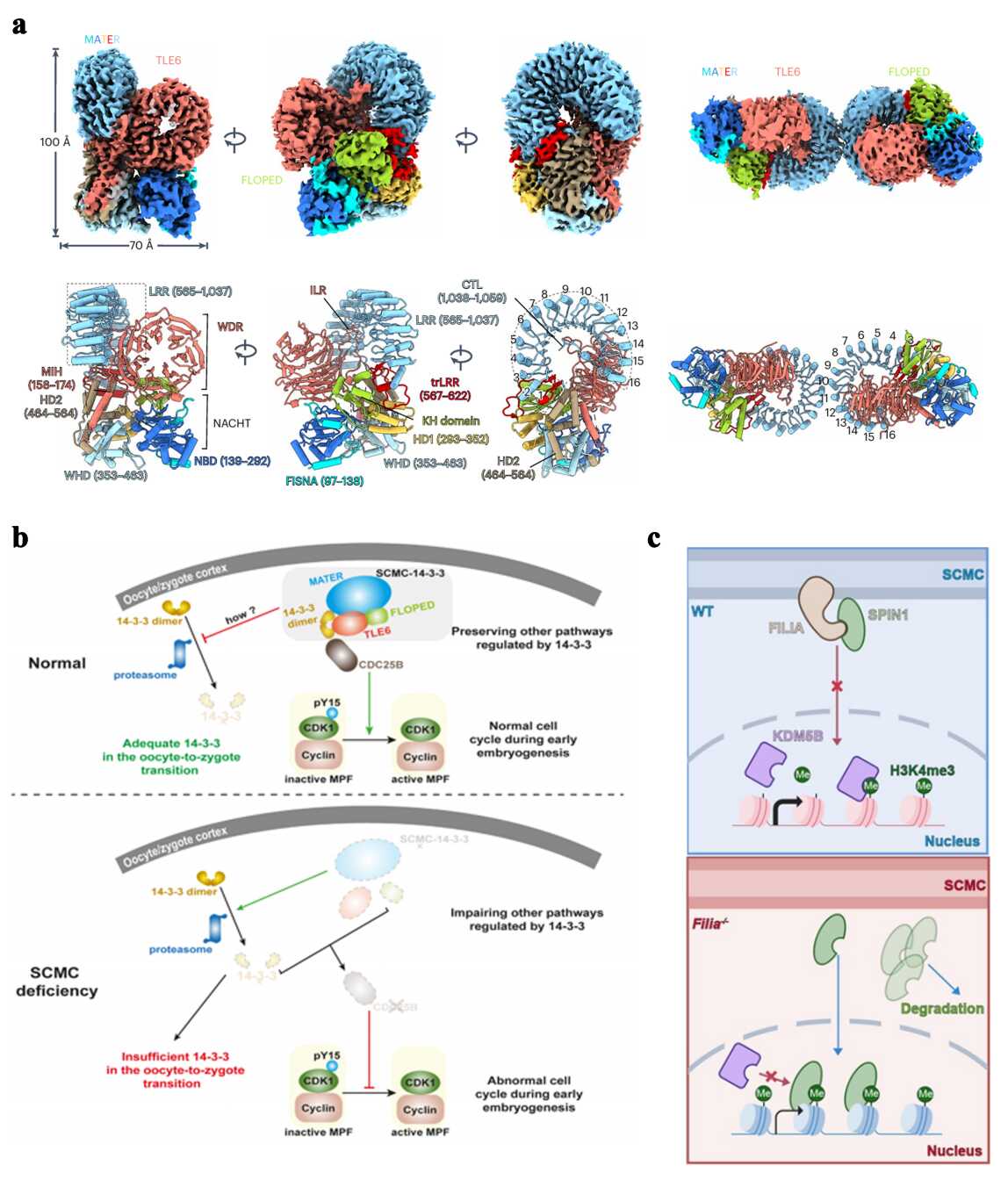
a. 小鼠SCMC核心复合体冷冻电镜结构。b. SCMC通过14-3-3调控哺乳动物早期胚胎细胞周期模式图。 c. SCMC调控小鼠早期胚胎表观修饰H3K4me3重编程的分子机制。
2.哺乳动物早期细胞谱系形成机制:哺乳动物早期胚胎发育是一个高度动态的生物学过程,而着床后的子宫内发育进一步增加了对其研究的难度。自上世纪八十年代第一株小鼠的胚胎干细胞(Embryonic Stem Cells, ESCs)建立以来,包括人类胚胎干细胞在内的多种类型的干细胞相继建立,为研究哺乳动物早期胚胎发育及干细胞临床应用提供可能。最近,我们建立了高效的哺乳动物早期胚胎培养体系,首次证明非人灵长类胚胎在没有子宫支持下可以发育至原肠胚,同时揭示了非人灵长类羊膜细胞的关键标记物,为研究灵长类原肠运动提供了重要平台(Science 2019);通过模拟胚胎发育环境,建立了第一株对应于哺乳动物原肠运动即将起动前上胚层细胞的活化态多能干细胞-fPSCs,它们不仅具有原肠运动启动前上胚层细胞的基因表达和表观修饰等特性,还可快速响应诱导信号进而分化为原始生殖细胞和三胚层的前体细胞,为研究早期胚胎细胞谱系建立提供了重要工具(Cell Research 2021);通过上述建立的高效哺乳动物早期胚胎培养和fPSCs研究体系,发现了多能干细胞从幼稚态向活化态转变过程中的重要调控网络,同时揭示了幼稚态调控网络清除的关键因子及其调控机制(Nucleic Acids Res 2022)。这些成果不仅加深了对哺乳动物早期胚胎细胞谱系形成的分子机制认识,还为哺乳动物早期胚胎发育研究提供了重要工具。
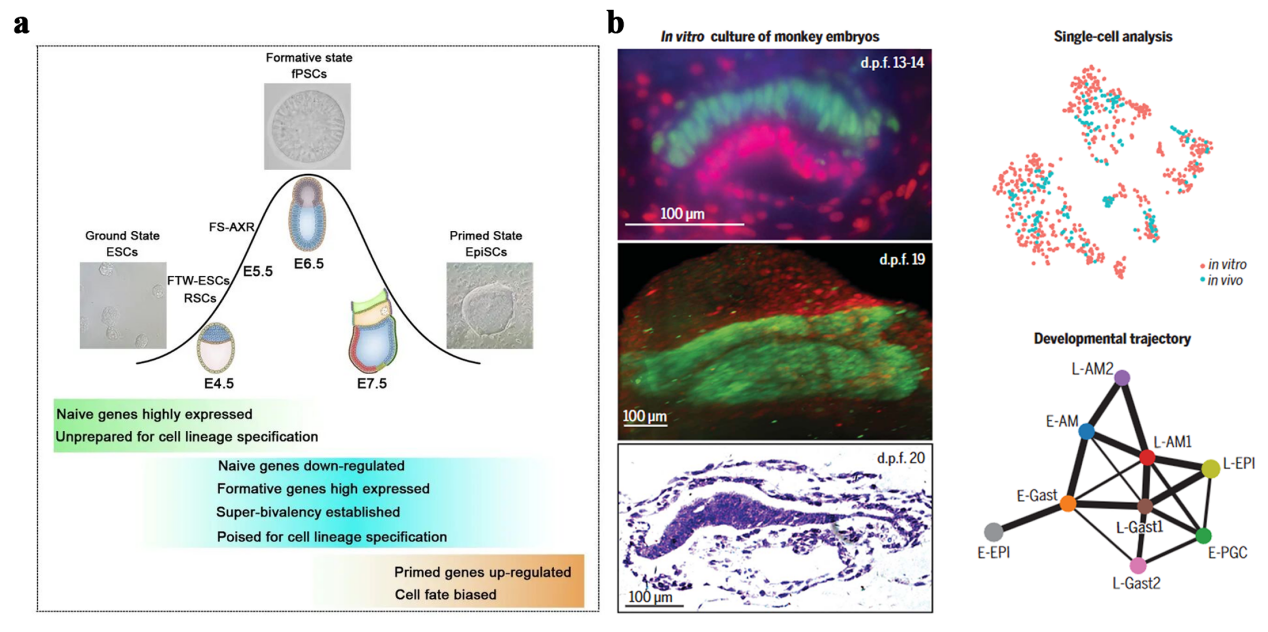
a. 新型活化态多能干细胞-fPSCs。 b. 原肠胚发育的体外研究模型。